INFECTIVE ENDOCARDITIS
Introduction
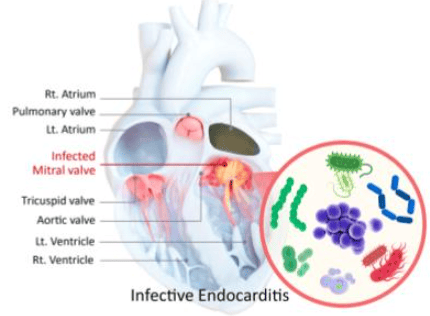
infective Endocarditis (IE) เป็นการติดเชื้อที่โครงสร้างของหัวใจ โดยเฉพาะที่บริเวณลิ้นหัวใจ รวมไปถึงบริเวณอุปกรณ์ทางการแพทย์ เช่น electrical cardiac device เป็นต้น ส่งผลให้มีการติดเชื้อในกระแสเลือด หรือเกิด Embolic phenomenal ตามมา เป็นภาวะที่พบไม่บ่อย แต่มีความรุนแรงนำไปสู่การเจ็บป่วยและเสียชีวิตอย่างรวดเร็ว หากไม่ได้รับการวินิจฉัยและรักษาอย่างมีประสิทธิภาพ
CLINICAL
Definite diagnosis
- Direct evidence: วินิจฉัย IE จากการตรวจเนื้อเยื่อ (histologic) หรือการเพาะเชื้อได้จาก vegetation หรือ embolized vegetation (กลุ่มของเกล็ดเลือด ไฟบริน และเชื้อก่อโรค) ที่ได้จากการผ่าตัด หรือ autopsy
- Clinical evidence: วินิจฉัย IE จากผลตรวจทั้งทางจุลชีววิทยา (microbiologic evidence) และ คลื่นไฟฟ้าหัวใจ (echocardiograph) โดยอ้างอิงตามเกณฑ์ Modified Duke Criteria เมื่อพบผลตรวจ 2 major criteria หรือ 1 major criteria ร่วมกับ 3 minor criteria หรือ 5 minor criteria
Modified Duke Criteria สำหรับวินิจฉัย IE
| Major criteria |
| 1.Microbiologic evidence: Blood cultures positive for IE |
a. Typical microorganisms consistent with IE detected from 2 separate blood cultures:
b. Microorganisms consistent with IE from persistently positive blood cultures:
c. Single positive blood culture for Coxiella burnetii, or anti-phase 1 IgG titer >1:800) |
| 2.Echocardiographic evidence: Imaging positive for IE |
a. Echocardiogram positive for IE:
b. Abnormal activity around the site of prosthetic valve implantation detected by 18FDG PET/CT (only if the prosthesis was implanted for >3 months) or radiolabeled leukocytes SPECTICT. |
| Minor criteria |
|
COMMON PATHOGENS
COMMON PATHOGENS
| ความเสี่ยงของการติดเชื้อ | เชื้อก่อโรคที่พบได้ |
|
Coagulase-negative staphylococci S. aureus Streptococci Enterococci S. bovis Fungi Gram-negative bacilli (กลุ่ม HACEK (Haemophilus spp., Aggregatibacter actinomycetemcomitans, Cardiobacterium hominis, Eikenella corrodens, และ Kingella kingae) |
|
S. aureus (including MRSA) Coagulase-negative staphylococci Enterococci Candida spp |
|
S. aureus (MSSA หรือ MRSA) Streptococci (viridans group) Coagulase-negative staphylococci Enterococci Gram-negative bacilli (เช่น P. aeruginosa) Candida spp. (ส่วนใหญ่ที่พบคือ C. albicans) |
TREATMENTS
General Principle
- การรักษาให้มีประสิทธิภาพ ประกอบด้วย endocardial vegetation eradication การป้องกันและรักษา
ภาวะแทรกซ้อนที่เกิดจากการติดเชื้อ และใช้ยาที่มีฤทธิ์เป็น bactericidal ในระดับยาสูงเพียงพอที่จะเข้าไปยัง vegetation โดยเลือกยาต้านจุลชีพที่เหมาะสม พิจารณาจากปัจจัยเสี่ยงของผู้ป่วย ชนิดและความไวของเชื้อก่อโรค - การรักษาด้วยยาปฏิชีวนะ พิจารณาตามชนิดของเชื้อก่อโรคเป็นหลัก (กรณีที่ยังไม่ทราบชนิดของเชื้อ และมีความ
จำเป็น เช่นผู้ป่วยมีอาการหนัก ให้พิจารณาใช้ Empiric therapy และปรับยาชนิดของยาเมื่อทราบชนิดเชื้อก่อโรค และความไวต่อยา (Susceptibility) - เพื่อการป้องกันการเกิดโรค การให้ยาปฏิชีวนะก่อนทำหัตถการในผู้เสี่ยงต่อการติดเชื้อมึความจะเป็น
Pathogen-directed: การให้ยาต้านจุลชีพ กรณีทราบเชื้อจุลชีพก่อโรค
1. เชื้อ viridians group streptococci และ S. bovis
| ขนาดยาและการบริหาร | ระยะเวลา | ข้อบ่งชี้-ข้อสังเกต |
| 1.1 เชื้อไวต่อ penicillin (AHA: MIC <0.125 mg/l) | ||
| • การรักษาแบบมาตรฐาน Monotherapy: – Penicillin G 12-18 million IU/day IV แบ่งให้ 6 ครั้งต่อวัน หรือ – Ceftriaxone 2 g/day IV/IM once daily หรือ – Amoxicillin 100-200 mg/kg/day IV แบ่งให้ 4-6 ครั้งต่อวัน |
4 สัปดาห์ |
แนะนําให้ในผู้ป่วยอายุ >65 ปี หรือในผู้ป่วย ที่มีไตทํางานบกพร่อง |
| • การรักษาระยะสั้น 2 สัปดาห์: Combination regimen: – Penicillin G หรือ ceftriaxone หรือ amoxicillin* ขนาดเดียวกันกับการรักษามาตรฐานนาน 2 สัปดาห์ ร่วมกับ – Gentamicin 3 mg/kyday IV/IM หรือ – Netitricin 4-5 mg/kg/day w* วันละครั้ง |
2 สัปดาห์ | กรณี non-complicated NVEประกอบด้วย: – ไม่พบ cardiac หรือ extracardiac abscess – มีการทํางานของไตปกติ – ไม่มีข้อบ่งชี้ของการผ่าตัด |
| 1.2 เขื้อดื้อต่อยา: Penicillin-relatively resistant (AHA: MIC 0.125 – < 0.5 mg/l; ESC:MIC 0.25 – 2 mg/l) | ||
| • Combination regimen: – Penicillin G 24 million IU/day IV แบ่งให้ 6 ครั้งต่อวัน หรือ – Ceftriaxone 2 g/day IV/IM once daily หรือ – Amoxicillin 100-200 mg/kg/day IV แบ่งให้ 4-6 ครั้งต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV/IM once daily |
4 สัปดาห์
2 สัปดาห์ |
|
| 1.3 กรณีผู้ป่วยแพ้ยา ß-lactam | ||
| • Monotherapy: – Vancomycin 30 mg/kg/day แบ่งให้ 2 ครั้งต่อวัน |
4 สัปดาห์ | กรณีเชื้อเป็น penicillin susceptible |
| • Combination regimen: – Vancomycin 30 mg/kg/day แบ่งให้ 2 ครั้งต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV/IM once daily |
4 สัปดาห์ 2 สัปดาห์ |
กรณีเชื้อเป็น penicillin relatively resistance |
2. เชื้อ Enterococcus spp. หรือ streptococci หรือเชื้อ nutritional variant streptococci
| ขนาดยาและการบริหาร | ระยะเวลา | ข้อบ่งชี้-ข้อสังเกต |
| 2.1 เชื้อไวต่อ ß-lactam และ gentamicin | ||
| • Combination regimen: – Ampicillin 12 g/day IV แบ่งให้ 6 ครั้งต่อวัน หรือ – Penicillin G 18-30 million IU/day IV แบ่งให้ 6 ครั้งต่อวัน หรือ – Amoxicillin 200 mg/kg/day IV แบ่งให้ 4-6 ครั้งต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV/IM แบ่งให้ 1-3 ครั้งต่อวัน |
4-6 สัปดาห์ |
พิจารณาให้การรักษา 4 สัปดาห์ถ้ามีอาการ <3 เดือน และรักษา 6 สัปดาห์ ถ้ามีอาการ >3 เดือน หรือ PVE |
| 2.2 เขื้อดื้อต่อยา: aminoglycoside ในระดับสูง (gentamicin MIC >500 mg) | ||
| • Combination regimen: – Ampicillin 12 g/day IV แบ่งให้ 6 ครั้งต่อวัน ร่วมกับ – Ceftriaxone 4 g/day IV แบ่งให้ 2 ครั้งต่อวัน |
6 สัปดาห์ | กรณีที่ผู้ป่วยมีการซื้อยา arinoglycoside |
| 2.3 กรณีผู้ป่วยแพ้ยา ß-lactam | ||
| • Combination regimen: – Vancomycin 30 mg/kg/day แบ่งให้ 2 ครั้งต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV/IM แบ่งให้ 1-3 ครั้งต่อวัน |
6 สัปดาห์ | กรณีที่ผู้ป่วยมีการซื้อยา arinoglycoside |
3. เชื้อ S. aureus
| ขนาดยาและการบริหาร | ระยะเวลา | ข้อบ่งชี้-ข้อสังเกต |
| 3.1 เชื้อไวต่อ Methicillin | ||
| • Combination regimen: – Cloxacillin 12 g/day IV แบ่งให้ 4-6 ครั้ง หรือ – Cotrimoxazole* SMX 4800 mg/day + TMP 960 mg/day
ร่วมกับ |
4-6 สัปดาห์ 6 สัปดาห์ 1 สัปดาห์ |
เป็น alternative therapy แนะนําจาก ESC guideline |
| 3.2 เชื้อดื้อต่อยา Methicillin (MRSA) | ||
| • Combination regimen: – Vancomycin 30 mg/kg/day แบ่งให้ 2 ครั้งต่อวัน ร่วมกับ – Rifampin 300 mg IV/PO q 8hr เป็นเวลา 6 wks ร่วมกับ – Gentamicin 1 mg/kg/day IV q 8hr เป็นเวลา 2 wks |
≥6 สัปดาห์ | |
| 3.3 กรณีผู้ป่วยแพ้ยา penicillin | ||
| • กรณีแพ้ยาแบบ non-anaphylaxis – Cefazolin 6 g/day IV แบ่งให้ 3 ครั้งต่อวัน หรือ – Cefotaxime* 6 g/day IV แบ่งให้ 3 ครั้งต่อวัน |
4*-6 สัปดาห์ | |
| • กรณีแพ้ยาแบบ anaphylaxis – Vancomycin 30 mg/kg/day แบ่งให้ 2 ครั้งต่อวัน |
4*-6 สัปดาห์ | |
* ESC: European Society of Cardiology
4. เชื้อกลุ่ม HACEK
| ขนาดยาและการบริหาร | ระยะเวลา | ข้อบ่งชี้-ข้อสังเกต |
| ยากลุ่ม ß-lactam | ||
| • Combination regimen: – Ceftriaxone 2 g/day IV หรือ – Ampicillin 12 g/day IV แบ่งให้ 4 หรือ 6 ครั้งต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV แบ่งให้ 2-3 ครั้งต่อวัน |
NVE: 4 สัปดาห์ PVE: 6 สัปดาห์ |
|
| – Ciprofloxacin 400 mg IV ทุก 8-12 ชั่วโมง หรือ 700 mg PO ทุก 12 ชั่วโมง |
กรณี Intolerant to ceftriaxone หรือ ampicillin | |
5. เชื้อ P. aeruginosa
| ขนาดยาและการบริหาร | ระยะเวลา | ข้อบ่งชี้-ข้อสังเกต |
| Preferred (จากข้อมูลผลการศึกษา invitro data) | ||
| • Combination regimen: – Piperacillin 4 g IV q 4h หรือ – Ceftazidime 2 g IV q 8h ร่วมกับ – Tobramycin 2.5 mg/kg IV q 8h (high dose, peak goal 15-20 mcg/m) |
4-6 สัปดาห์ |
ส่วนใหญ่พบในกลุ่มผู้ใช้ยาเสพติดชนิดฉีด (ข้อเสนอแนะยาต้านจุลชีพ จากข้อมูลผลการศึกษา invitro data) |
| Alternatives | ||
| • Combination regimen: – ß-lactam หรือ Fluoroquinolone หรือ Carbapenem ตัวใดตัวหนึ่ง
ร่วมกับ
|
4-6 สัปดาห์ |
ส่วนใหญ่พบในกลุ่มผู้ใช้ยาเสพติดชนิดฉีด (ข้อเสนอแนะยาต้านจุลชีพ จากข้อมูลผลการศึกษา invitro data) |
Empirical Therapy: การให้ยาต้านจุลชีพ กรณีไม่ทราบเชื้อจุลชีพก่อโรค
| Antibiotic dosage and route |
| NVE และ Late PVE (NVE: Community-acquired native valve IE; Late PVE: ≥ 12 months post-surgery IE) |
| • Combination#1 – Ampicillin 12 g/day IV แบ่งให้ 4 หรือ 6 ครั้งต่อวัน ร่วมกับ – (Flu) cloxacillin or oxacillin 12 g/day IV แบ่งให้ 4 หรือ 6 ครั้งต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV/IM once daily |
| • Combination#2 – Vancomycin 30-60 mg/kg/day IV แบ่งให้ 2-3 doses ต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV/IM once daily |
| Early PVE, nosocomial หรือ non-nosocomial healthcare associated IE (Early PVE: < 12 months post-surgery IE) |
| • Combination – Vancomycin 30 mg/kg/day IV แบ่งให้ 2 doses ต่อวัน ร่วมกับ – Gentamicin 3 mg/kg/day IV/IM once daily ร่วมกับ – Rifampin 900-1200 mg IV/PO แบ่งให้ 2-3 doses ต่อวัน |
ANTIBIOTIC FOR IE PROPHYLAXIS
Indications
Patient Indication: ผู้ป่วยกลุ่มเสี่ยงที่จำเป็นต้องพิจารณาให้ยาป้องกันการติดเชื้อ
| Risk to IE | Antibiotic prophylaxis |
| Highest risk 1. ผู้ป่วยที่มีประวัติดังนี้
2. ผู้ป่วยที่เคยมีประวัติเป็น IE มาก่อน 3. ผู้ป่วยที่มีโรตประจำตัวดังนี้
|
Recommended. |
| Intermediate risk ผู้ป่วยมีภาวะ CHD หรือ native valve disease ในลักษณะอื่น |
NOT Recommended |
Procedure Indication: หัตถการที่ผู้ป่วยกลุ่มเสี่ยงจำเป็นต้องได้รับยาป้องกันการติดเชื้อ
| IE Risk by Procedure Indication | Antibiotic prophylaxis |
| Highest risk | |
1. Dental: มีลักษณะต่อไปนี้
2. Non-dental: มีลักษณะต่อไปนี้
|
Recommended. |
| No risk | |
1. Dental ที่ไม่มีความเสี่ยง ได้แก่
2. Non-dental ที่ปัจจุบันพบว่าไม่มีความเสี่ยง และไม่อยู่ในข่ายให้ยาป้องกัน ประกอบด้วย GI, reproductive organ and GU |
NOT Recommended EXCEPT invasive procedure |
Recommended Antibiotic Prophylaxis Regimens
Recommended prophylaxis สำหรับ High-risk dental procedures ในผู้ป่วยเสี่ยงสูง
| Situation | Antibiotic | Single-dose 30-60 minutes before procedure | |
| Adults | Children | ||
| No allergy to penicillin or ampicillin | Amoxicillin or ampicillin | 2 g orally or IV | 50 mg/kg orally or IV |
| Allergy to penicillin or ampicillin | Clindamycin | 600 mg orally or IV | 20 mg/kg orally or IV |
| a Alternatively: Cephalexin 2 g IV for adults or 50 mg/kg IV for children, Cefazolin or ceftriaxone 1 g IV for adults or 50 mg/kg IV for children Cephalosporins should not be used in patients with anaphylaxis, angio-oedema, or urticaria after intake of penicillin or ampicillin due to cross-sensitivity. |
|||
Recommended prophylaxis สำหรับ Non-dental invasive procedures ในผู้ป่วยเสี่ยงสูง
Systemic antibiotic prophylaxis is not recommend for non-dental procedure EXCEPT invasive procedure
| Respiratory tract procedures | GI/GU procedures | Dermatological & Musculoskeletal procedures |
|
| Indication | Invasive procedure to treat established infection: • Drainage |
|
Involved:
|
| Antibiotics | Antibiotics Against staphylococcal drug | Against enterococci
|
Against:
|
OTHER RESOURCES
OTHER RESOURCES
https://www.ncbi.nlm.nih.gov/books/NBK557641/
https://www.researchgate.net/figure/Summary-of-current-literature-surrounding-infective-endocarditis-complicating_fig1_338566432
References
[1] Paul G. Auwaerter and John G. Bartlett, “Endocarditis – Prosthetic valve; Endocarditis – Injecting drug users,” in The John Hopkins POC-IT ABX Guide, Handover MD, The Johns Hopkins University POC-IT Center, 2020-2022.
[2] Aaron W. Yallowitz; Lawrence C. Decker, “Infectious Endocarditis,” 24 April 2023. [Online]. Available: https://www.ncbi.nlm.nih.gov/books/NBK557641/. [Accessed 08 November 2023].
[3] ณสิกาญจน์ อังคเศกวินัย, “Cardiovascular Infections: Infective Endocarditis,” in Handbook of Infectious Disease [Editor: รุจิภาส สิริจตุภัทร ภาคภูมิ พุ่มพวง วลัยพร วังจันดา], 2nd ed., กรุงเทพมหานคร, สาขาวิชาโรคติดเชื้อและอายุรศาสตร์เขตร้อน ภาควิชาอายุรศาสตร์ คณะแพทยศาสตร์ ศิริราชพยาบาล มหาวิทยาลัยมหิดล, 2021, pp. 131-137.
[4] Habib G, Lancellotti P, Antunes MJ, Bongiorni MG, Casalta JP, Del Zotti F, et al., “ESC Guidelines for the management of infective endocarditis (Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS) and the European Association of Nuclear Medicine (EANM),” Eur Heart J., vol. 36, no. 44, pp. 3075-128, 2015.
[5] Sasitorn Sakkarat and Pongsanae Duangpakdee, “Infective endocarditis,” 21 June 2018. [Online]. Available: http://medinfo2.psu.ac.th › surgery. [Accessed 26 June 2023].
[6] Wapcaplet, CC BY-SA 3.0 <http://creativecommons.org/licenses/by-sa/3.0/>, “Wikimedia Commons,” [Online]. Available: https://commons.wikimedia.org/wiki/File:Diagram_of_the_human_heart_(cropped).svg.
